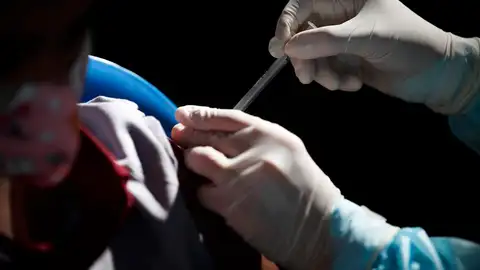
la EMA (Agencia Europea del Medicamento) ha recomendado extender el uso de las vacunas mRNA dirigidas a la cepa original de SARS-CoV-2. El Comité ha recomendado administrarla en niños de 6 meses a 4 años para Comirnaty (Pfizer) y el uso en niños de 6 meses a 5 años para Spikevax (Moderna). Comirnaty y Spikevax ya están aprobadas tanto en adultos como en niños de 5 y 6 años, respectivamente.
Dosis a los niños
Las dosis serán menores que en las vacunas para adultos. En niños de 6 meses a 4 años de edad, Comirnaty puede administrarse como vacunación primaria que consta de tres dosis (de 3 microgramos cada una); las dos primeras dosis se administran con tres semanas de diferencia, seguidas de una tercera dosis administrada al menos 8 semanas después de la segunda dosis. En niños de 6 meses a 5 años de edad, Spikevax puede administrarse como vacunación primaria que consta de dos dosis (de 25 microgramos cada una), con cuatro semanas de diferencia. Ambas vacunas se administrarán en la parte superior del brazo o del muslo.
Posibles efectos secundarios
Los efectos secundarios más comunes de ambas vacunas, en niños de 6 meses a 4 o 5 años, fueron comparables a los observados en grupos de mayor edad. Irritabilidad, somnolencia, pérdida de apetito, sarpullido y sensibilidad en el lugar de la inyección. Para ambas vacunas, estos efectos fueron generalmente leves o moderados y mejoraron a los pocos días de la vacunación.
La EMA ha concluido que los beneficios de vacunar a niños de 6 meses a 4 y 5 años superan ampliamente a los riesgos. La seguridad y eficacia de ambas vacunas, en niños y adultos, continuarán siendo monitoreadas de cerca. La EMA enviará ahora sus opiniones científicas a la Comisión Europea, que será quien tome la última decisión sobre la ampliación de la licencia de uso para estos nuevos grupos de edad.